
從細胞到個體、從個人到群體、從人群到動物、從體內保健到生態環保,GMI免疫調節蛋白全面地提供了良性循環的基礎。
GMI免疫調節蛋白有高度的協同性、安全性及有效性,已具備新藥開發的資格。
中山醫學大學柯俊良教授團隊2025年底發表的研究證明,不論EGFR雙突變的肺腺癌細胞是否已經對第三代標肥藥奧希替尼 ( 泰格莎 ) 產生抗藥性,GMI都能透過「促凋亡」和「促自噬」降低癌細胞的存活與增殖能力。柯教授提及本研究的起心動念是源於某交演講,有聽眾問起:「GMI對奧希替尼這個藥物會有影響嗎?在奧希替尼產生抗藥性之後還有幫助嗎?」才會發想本研究來進行探討,提供科學證據來證實GMI的功效。
EGFR基因突變在肺腺癌相當常見。當EGFR出現雙重突變時,癌細胞往往會對第一、二代EGFR標靶藥產生抗藥性,雖然目前已有專門針對此類突變設計的第三代EGFR標靶藥——奧希替尼(osimertinib,商品名:泰格莎【Tagrisso】)可供治療,但是部分患者從一開始就對藥物反應不佳;即使是初期療效良好的病人,在治療一段時間後,最終也會產生抗藥性。
面對這種一再突變的癌細胞,除了等待第四代EGFR標靶藥問世之外(如果時間允的話),或回到傳統的化療方法(如果身體允許的話),現成的小孢子靈芝免疫調節蛋白質GMI(Ganoderma microsporum immunomodulatory protein)也許是值得一試的另類辦法。
根據2025年底發表在北歐藥理學與毒理學協會官方刋物《基礎與臨床藥理學與毒理學》(Basic & Clinical Pharmacology & Toxicology) 的研究顯示,不論EGFR雙突變的肺腺癌細胞是否已經對奧希替尼產生抗藥性,GMI都能透過「促凋亡」和「促自噬」雙重手段,大幅降低癌細胞的存活與增殖能力。
該研究由中山醫學大學醫學研究所柯俊良教授、辛翌綸博士後研究員率領的團隊,聯手中山醫學大學醫學檢驗暨生物技術學系蔡振寧副教授,以及台中榮民總醫院康于庭高級助理研究員等共同完成。
柯俊良教授提及本研究的起心動念是源自某次演講,當時有聽眾問起G M I對奧希替尼(泰格莎)這個藥物會有影響嗎?以及在奧希替尼產生抗藥性之後還有幫助嗎?才會發想本研究來進行探討,提供科學證據來證實GMI的功效。
針對EGFR雙突變的肺腺癌細胞開發的第三代標靶藥——奧希替尼(泰格莎)
在繼續解說GMI如何透過「促凋亡」和「促自噬」對付EGFR雙突變肺腺癌細胞之前,讓我們先了解一下「EGFR雙突變」和奧希替尼代表的意義。
簡稱EGFR的「表皮生長因子受體」是一種橫跨細胞膜的受體蛋白。當它接收到外來生長訊號的刺激時,會啟動細胞內一連串相關的訊號傳遞反應,促使細胞增生。正常細胞會嚴格調控EGFR的表現量和活性,但在某些狀況下,EGFR基因可能會發生突變(如L858R或 Ex19del突變),使EGFR持續處於活化狀態,毋須外來刺激就能全天候驅動細胞增生。
第一、二代EGFR標靶藥便是針對這類EGFR持續活化的突變所開發,但通常在治療一段時間後,EGFR又會進一步出現抗藥性突變(T790M突變),使藥效下降。為了對付這種增生速度快、且對前兩代標靶藥產生抗藥性的「EGFR雙突變」癌細胞,後來又有第三代標靶藥奧希替尼問世。
奧希替尼對常見的EGFR突變(Ex19del、L858R、T790M)皆具有抑制效果,因此除了適用於治療具有EGFR產生T790M基因突變而導致第一、二代EGFR標靶藥失效的非小細胞肺癌病人之外,現也成為第一線治療藥物,用來治療EGFR突變、但不一定具有T790M突變之非小細胞肺癌病人。
EGFR雙突變的肺腺癌細胞 其存活與增殖能力會因GMI介入而降低
本研究使用的人類肺腺癌細胞H1975為具有EGFR雙突變(L858R/T790M)且對奧希替尼敏感(奧希替尼治療有效)的特性;而人類肺腺癌細胞H1975/TR則是具有EGFR雙突變但對奧希替尼有抗藥性的特性。
把這兩種肺腺癌細胞跟不同劑量的GMI一起培養24~48小時,結果發現,兩種癌細胞的存活率都會依GMI濃度的增加而下降,(圖1),而且只需0.6 μM的GMI幾乎就能完全抑制兩種癌細胞的增殖能力(圖2)。這說明這兩種癌細胞對GMI有相近的敏感度,即使是奧希替尼治療不動的癌細胞,GMI依然有效。
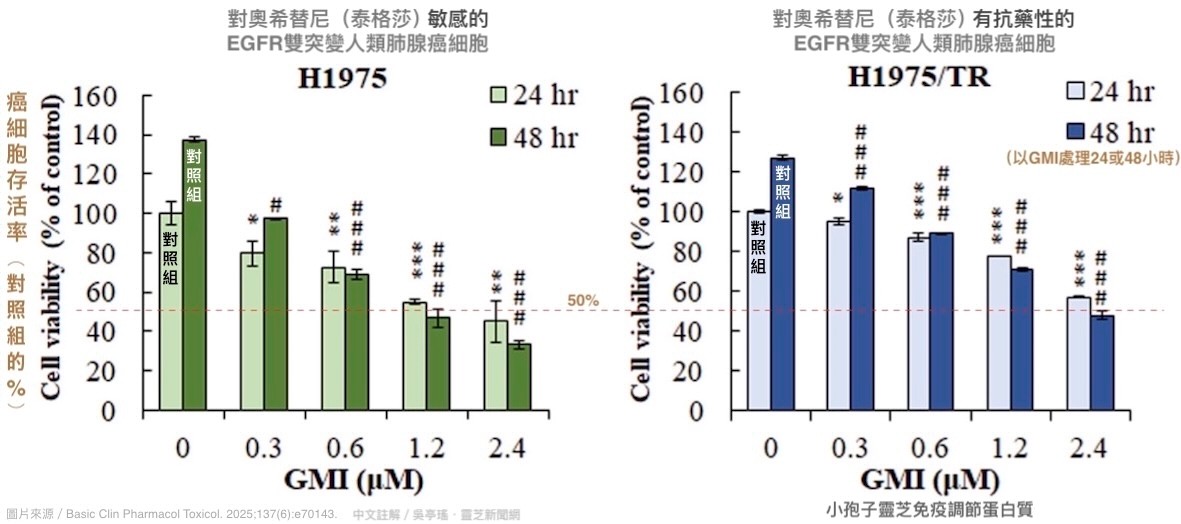
【圖1】GMI可降低EGFR雙突變人類肺腺癌細胞的存活能力
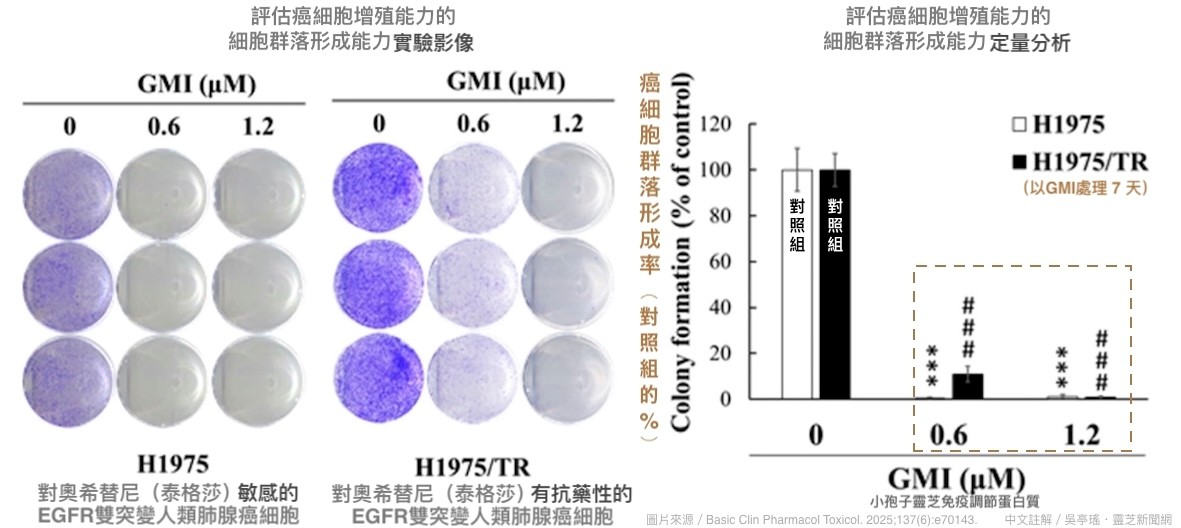
【圖2】GMI可降低EGFR雙突變人類肺腺癌細胞的增殖能力
註:圖1和圖2標示✽和#者表示,與同時間未以GMI處理的對照組相比,有顯著差異。
GMI「促凋亡」和「促自噬」雙管齊下 誘導EGFR雙突變肺腺癌細胞走向死亡
研究還發現,GMI會「促凋亡」和「促自噬」雙管齊下,來誘導這兩種EGFR雙突變肺腺癌細胞死亡,只是「技巧上」有些差異:
對奧希替尼敏感的肺腺癌細胞H1975,GMI是以「促進細胞凋亡」為主要手段;對奧希替尼有抗藥性的肺腺癌細胞H1975/TR,GMI則是以「促進細胞自噬」為主要手段(圖3)。
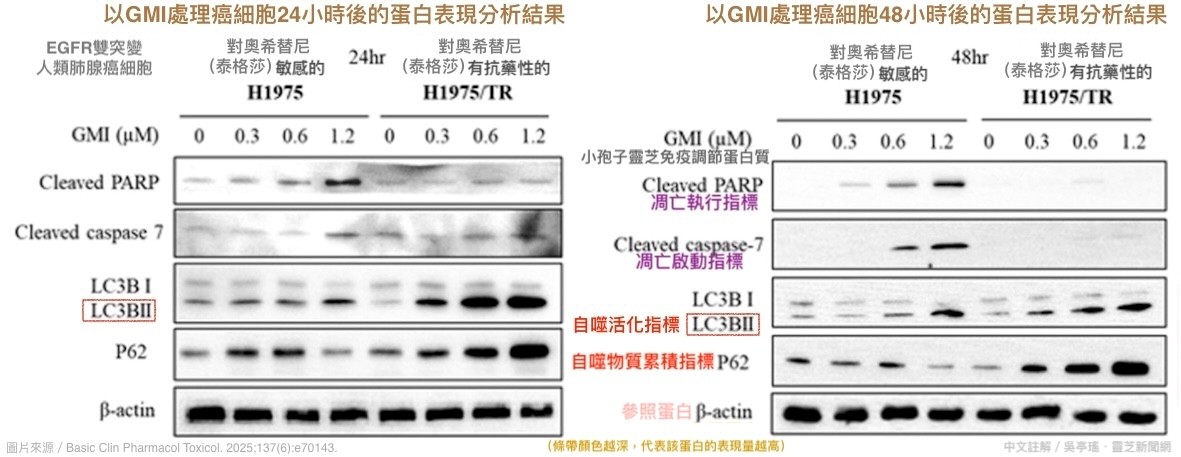
【圖3】GMI可誘導EGFR雙突變人類肺腺癌細胞凋亡或自噬
❖當細胞出現cleaved caspase-7(裂解的/活化的凋亡蛋白7)時,代表凋亡程序已經啟動且不可逆轉。
❖PARP是修復DNA的蛋白酶,cleaved caspase-7會切割PARP(成為cleaved PARP),使細胞失去修復能力而走向死亡,因此cleaved PARP的出現,代表凋亡程序已在執行中,細胞即將死亡。
❖細胞自噬程序啟動後,會把準備送去資源回收場分解的東西包起來,形成囊泡狀的「自噬體」,由於自噬體膜上有LC3B-II蛋白標誌物,故將其視為自噬活化的指標。
❖p62的累積暗示自噬體因資源回收場消化不及而大量堆積在細胞裡,表示細胞在自噬過程承受過量的負荷,可能進一步引發細胞死亡。
❖β-actin是一種在細胞中穩定存在的結構蛋白,常在蛋白表現量檢測中,被當作內部對照,用來確認各組樣本加入的蛋白量一致。
細胞凋亡&細胞自噬的意義
「細胞凋亡」是細胞內建的計畫性死亡機制,當細胞老化或出現異常時,這個機制便會主動開啟。正常細胞就是藉此汰舊換新,但癌細胞則會想方設法「抗凋亡」,故能永生不死,並持續保持增殖的活力。
「細胞自噬」則是細胞在壓力或飢餓脅迫下的求生機制,正常細胞和癌細胞都能在情急之下使出這種大絕招,透過吞噬細胞本身比較不重要或受損的胞器,暫時維持生存,但最後是死是活,得看危機解除前細胞能否撐得住。
因此,不論是重新啟動癌細胞的凋亡機制,或是誘導癌細胞自噬而亡,都能阻止癌細胞生長、降低癌細胞數量,進而有機會使癌症從「失控」變得「可控」。由於細胞凋亡與細胞自噬原本都是正常細胞可能經歷的生理過程,因此當癌細胞透過這些機制走向死亡時,通常比較不易引發強烈的發炎反應。
所以「促凋亡」和「促自噬」雙管齊下的GMI,可說是用一種相對溫和的方式在清除癌細胞。我們甚至可以從圖3顯示的分析結果推測,當GMI誘導的細胞凋亡對抗藥性H1975/TR細胞不太管用時,主導細胞死亡的機制似乎很快就改從自噬途徑下手。
而癌細胞最後之所求生不得,很可能是因為形成的自噬體太多,使得負責分解消化的資源回收系統超載,以致整個細胞功能被拖垮。
GMI可以把作怪的EGFR消失或變弱 EGFR標靶藥的作用機制不同
研究團隊還發現,當EGFR雙突變肺腺癌細胞H1975跟GMI一起培養24小時之後,不僅EGFR表現量減少(以至沒有EGFR可供活化),細胞內部與EGFR相關的訊號傳遞也明顯受到抑制(圖4),這些作用都會導致癌細胞失去維持存活的訊號支持,進而啟動細胞凋亡程序。
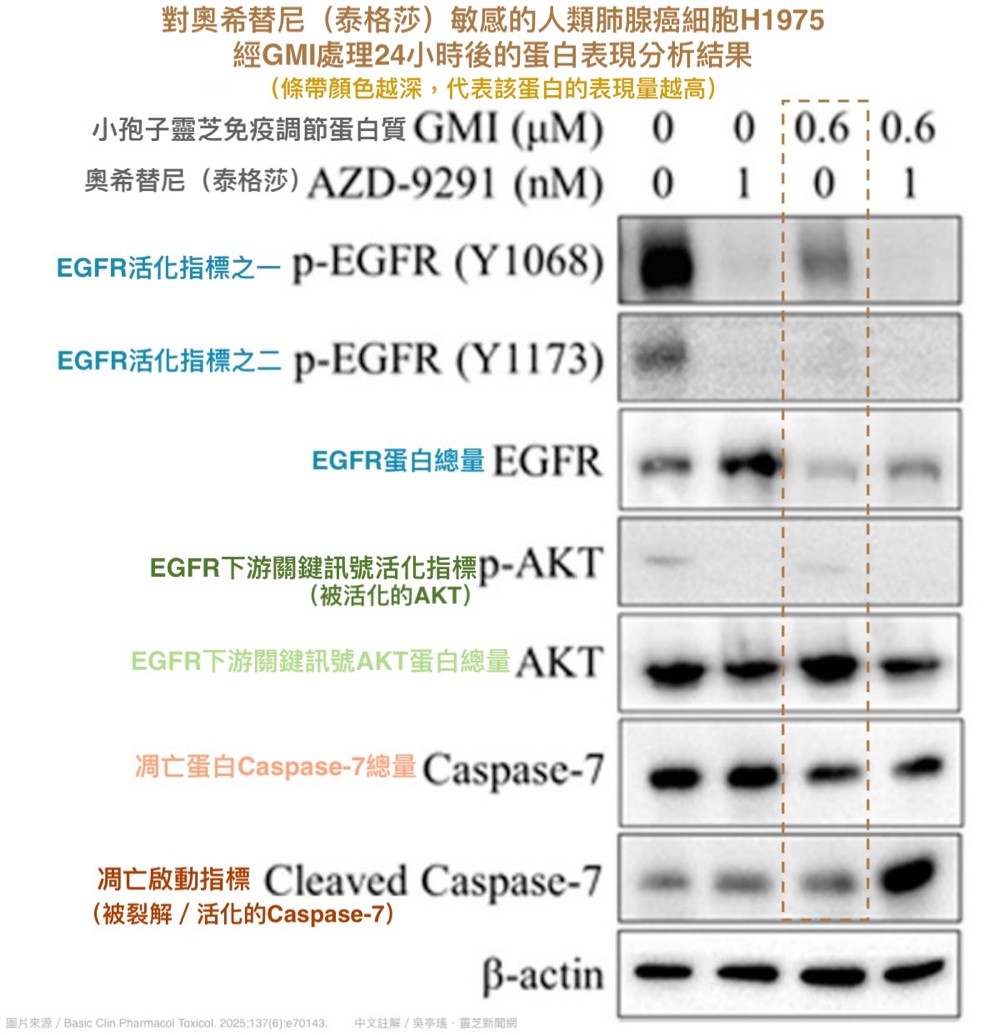
【圖4】對於EGFR雙突變人類肺腺癌細胞H1975
GMI可減少EGFR並降低其下游訊號的活化程度
註:圖中的EGFR(Y1068)和EGFR(Y1173)是指EGFR被活化(磷酸化)的訊號位置,當它們的活化代表EGFR處在活性狀態。
至於對奧希替尼有抗藥性的EGFR雙突變肺腺癌細胞H1975/TR,GMI同樣可以抑制EGFR及其下游相關訊號的活化。這說明GMI雖然也是標靶EGFR,但其作用機制跟奧希替尼並不相同。而H1975/TR細胞很可能也是在賴以為生的EGFR訊號被GMI削弱後,才走向死亡。
目前用於臨床的EGFR標靶藥,不管是第一代、第二代,或本研究聚焦的第三代的奧希替尼(泰格沙),都是針對EGFR位於細胞內側的酪胺酸激酶活性進行抑制,而癌細胞也可以讓EGFR一再突變,不斷產生新的抗藥性。
但GMI的作用機制則跟酪胺酸激酶無關。根據先前研究可知,GMI可以跟細胞表面的EGFR結合,促使其被細胞內吞並進一步降解。很可能就是因為如此不同的作用機制,讓GMI可以克服EGFR癌細胞的抗藥性問題,把原本失控的癌症變得可控。
由於研究團隊先前發表另一項研究證明,GMI可以透過「清除整合素」有效抑制EGFR雙突變肺腺癌細胞的遷移能力——不管癌細胞是否對奧希替尼有抗藥性;如今再加上本研究聚焦的「促凋亡」和「促自噬」,以及兩個研究都有提及的「清除EGFR或削弱相關訊號」,GMI這套四面夾殺的組合拳打下來,可真會讓這種「很會逃」的癌細胞也難逃法網。
附註
①第一代EGFR標靶藥包括:吉非替尼(gefitinib,商品名艾瑞莎 [Iressa])、厄洛替泥(erlotinib,商品名得舒緩 [Tarceva])。
②第二代EGFR標靶藥包括:阿法替尼(afatinib,商品名妥復克 [Giotrif])。
③ EGFR突變:由於EGFR基因發生變異,使EGFR蛋白結構出現改變。這些看似微小的變化,卻可能影響EGFR標靶藥與EGFR的結合能力,進而導致抗藥性產生。
❖ L858R突變代表EGFR蛋白第858個胺基酸由L(亮胺酸)轉變為R(精胺酸),會使EGFR持續處於活化狀態,通常可被第一代或第二代EGFR標靶藥抑制。
❖ Ex19del突變代表EGFR基因第19號外顯子的一小段序列發生缺失,導致EGFR蛋白局部結構縮短並持續活化,亦通常可被第一代或第二代EGFR標靶藥抑制。
❖ T790M突變代表EGFR蛋白第790個胺基酸由T(蘇胺酸)轉變為M(甲硫胺酸),會降低第一代與第二代EGFR標靶藥的抑制效果,使癌細胞產生抗藥性。
④ 源自小孢子靈芝(Ganoderma microsporum)的GMI是一個化學結構清楚且可被規模化量產的純蛋白質,其在蛋白質資料庫Protein Data Bank(PDB ID: 3KCW) 和美國衛生研究院的化學分子與生物活性資料庫PubChem(SID:461501955)均登記有案。
其安全性已在亞慢性毒性、致畸性和遺傳毒性研究中獲得證明(2022年發表)。2020年被美國FDA列為無保留意見的新膳食成分(NDI1133),2022年再被台灣衛福部核准為【可供食品使用原料】,說明GMI具備高度的食用安全性;其在在體內的抗腫瘤效果——不論口服或注射——也獲得許多研究和實際經驗支持。
.png)
【圖5】小孢子靈芝免疫調節蛋白質GMI的化學結構
全文轉載自靈芝新聞網:柯俊良團隊2025研究成果|促凋亡&促自噬——小孢子靈芝免疫調節蛋白質GMI左右開弓抑制EGFR雙突變肺腺癌